Medicina del futuro, Antiaging, Epigenetica e Biomarcatori
TEORIE > CONCETTI > MEDICINA E GENETICA
Scopo di questa pagina
La medicina del futuro sta cambiando paradigma, abbandonando il paradigma reattivo per intraprendere quello predittivo. Questo processo è previsto si completi entro una decina d'anni e avverrà in parallelo con i processi antiaging, sull'onda della rivoluzione 'omica' e dello sviluppo di orologi epigenetici sempre più precisi. Per capire cosa succederà dobbiamo capire com'è fatto l'organismo umano, e quindi il fenotipo. In genetica, il fenotipo (dal greco antico φαίνω (phaínō) 'apparire, mostrare, risplendere', e τύπος (túpos) 'marchio, tipo') è l'insieme delle caratteristiche o tratti osservabili di un organismo. Il termine riguarda la morfologia dell'organismo (forma fisica e struttura), i suoi processi di sviluppo, le sue proprietà biochimiche e fisiologiche. Il fenotipo deriva da due fattori fondamentali: l'espressione del codice genetico dell'organismo (il suo genotipo) e l'influenza dei fattori ambientali. Entrambi i fattori possono interagire, influenzando ulteriormente il fenotipo. Il fenotipo di un organismo non comporterà solo le caratteristiche osservabili come la morfologia, ma includerà anche molecole e strutture come l'RNA e le proteine prodotte come codificate dai geni; questo è indicato come "fenotipo molecolare". La genetista Angela Brooks-Wilson scrive (2013): "L'ereditabilità dell'età alla morte in età adulta è di circa il 25%. L'epigenetica sta rapidamente emergendo come un aspetto critico dell'invecchiamento e della longevità."
Cos'è un fenotipo
Si potrebbe dire che il fenotipo si confronta col mondo,
mentre il genotipo 'pianifica' il fenotipo e la sua 'resilienza' nel mondo
mentre il genotipo 'pianifica' il fenotipo e la sua 'resilienza' nel mondo
"Pheno" significa semplicemente "osservare" e deriva dalla stessa radice della parola "fenomeno". E quindi è una tipologia osservabile di un organismo, e può riferirsi a qualsiasi cosa, da un tratto comune, come l'altezza o il colore dei capelli, alla presenza o all'assenza di una malattia. Ma è importante ricordare che i fenotipi sono ugualmente, o talvolta anche più fortemente influenzati dagli effetti ambientali rispetto agli effetti genetici. Di solito non c'è una correlazione uno a uno tra un genotipo e un fenotipo, perchè ci sono quasi sempre influenze ambientali, quali, ad esempio, ciò che si mangia, quanto ci si esercita fisicamente, quanto si fuma, quanto alcol si beve, ecc. Tutte queste sono influenze ambientali che determineranno il fenotipo.
Ogni fenotipo è fortemente influenzato, più che dalla sua eredità genetica dalle sue influenze ambientali, cioè dagli stress cui l'organismo è sottoposto nel corso della vita.
Che cosa influenza il fenotipo
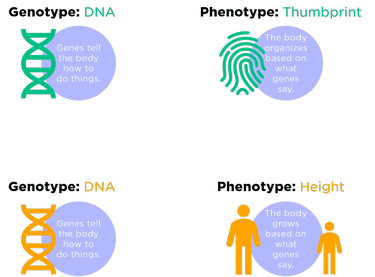
Non c'è una correlazione uno a uno tra un genotipo e un fenotipo, perchè ci sono quasi sempre influenze ambientali,
quali, ad esempio, ciò che si mangia, quanto ci si esercita fisicamente, quanto alcol si beve, quanto si fuma, ecc.
Tutte queste sono influenze ambientali che influenzeranno il fenotipo.
Per capire di cosa si compone la resilienza di ogni individuo, alla quale è affidato il suo invecchiamento sano, in biologia è in corso la rivoluzione 'omica'. Infatti “Genoma” è una parola ormai piuttosto conosciuta, anche per merito del Progetto Genoma Umano, che 20 anni fa ci ha consegnato la prima bozza della sequenza di lettere che compongono il nostro DNA. Ma se dicessimo “trascrittoma”? Oppure “proteoma” o, ancora, “metaboloma”? Sono parole certo meno familiari, eppure è facile accorgersi che hanno tutte qualcosa in comune e cioè quelle tre lettere finali - oma - che indicano una totalità. Ciascuno di questi termini, dunque, si riferisce all’insieme totale di qualcosa che si può trovare in un tessuto, un organismo o anche una singola cellula. Sono sequenze di DNA per il genoma, trascritti (cioè molecole di Rna) per il trascrittoma, proteine per il proteoma, metaboliti (piccole molecole coinvolte nelle varie vie biochimiche di una cellula) per il metaboloma. E così via. Le tecniche utilizzate per studiare questi insiemi, invece, prendono il nome di "omiche" (genomica, trascrittomica, proteomica ecc.) e rappresentano una delle avanguardie più promettenti della ricerca biologica. La proteomica e la metabolomica, le discipline più “a valle” tra tutte le scienze “omiche”, sono da considerarsi quelle più vicine all’espressione fenotipica di un organismo, poiché rispecchiano sia l’informazione contenuta nel codice genetico sia le influenze derivate dall’interazione con l’ambiente. La metabolomica è stata ideata nel 1970 da Arthur B. Robinson il quale, analizzando i modelli cromatografici "confusi" di urina di soggetti a cui era stata somministrata la Vitamina B6, si rese conto che centinaia o migliaia di costituenti chimici nell'urina contenevano informazioni molto utili. Dal 1971 Robinson ha fatto pubblicare altri diciannove elaborati sui modelli quantitativi degli umori corporei. Queste nuove metodologie basate sulla genetica, metabolomica e proteomica permettono di avere a disposizione un consistente numero di nuovi biomarker. Il loro utilizzo nella ricerca clinica è una realtà in atto, mentre l’uso nella pratica clinica è ancora parziale.
La proteomica e la metabolomica, sono da considerarsi le tecnologie più vicine all’espressione fenotipica di un organismo, poiché rispecchiano sia l’informazione contenuta nel codice genetico sia le influenze derivate dall’interazione con l’ambiente.
La rivoluzione 'omica'
Le scienze omiche (omics) sono una delle avanguardie più promettenti della ricerca biologica
I progressi nella tecnologia ad alto rendimento offrono nuove opportunità per la ricerca omica per comprendere il processo patologico di varie malattie umane complesse. Le tecnologie single-omics forniscono solo informazioni limitate sui meccanismi biologici delle malattie. DNA, RNA, proteine, metaboliti e microrganismi di solito svolgono ruoli complementari e svolgono insieme determinate funzioni biologiche. Ma cos'è un biomarcatore? Maria Salud Garcia-Gutierrez scrive (vedi bibliografia 2020): "Al fine di armonizzare il termine di biomarcatore, la Food and Drug Administration (FDA) in collaborazione con il NIH Joint Leadership Council ha convocato il gruppo di lavoro sui biomarcatori FDA-NIH nel 2016. Questo gruppo ha semplificato la definizione di biomarcatore essendo considerato come "una caratteristica definita che è misurato come un indicatore di normali processi biologici, processi patogeni o risposte a un'esposizione o intervento”. Questa definizione, più chiara e concisa, definisce un biomarcatore specificandone le principali applicazioni senza inutili complessità o informazioni contraddittorie. Inoltre, per garantirne l'uso clinico, un buon biomarcatore dovrebbe essere misurato con elevata riproducibilità, presentare un rapporto segnale/rumore considerevole e, soprattutto, soddisfare la condizione di essere modificato in modo dinamico e affidabile con il progredire della condizione clinica. Inoltre, un biomarcatore dovrebbe essere accessibile per la sua rilevazione e misurazione, come nel caso di un parametro plasmatico o di un marcatore genetico, o essere rilevato mediante tecniche istologiche o di immagini/neuroimmagini ":
Negli ultimi anni il settore dei biomarker nella ricerca e nella pratica clinica ha avuto notevoli progressi. Questi test possono essere utilizzati per il monitoraggio delle malattie: screening, diagnosi, prognosi, ecc. come pure per misurare lo stato d'invecchiamento del fenotipo e gli effetti degli interventi nutraceutici nel tempo.
Tipologie di biomarcatori

Un biomarcatore, o marcatore biologico, si riferisce generalmente a un indicatore misurabile di qualche stato o condizione biologica. Potenziali biomarcatori tra cui proteine e frammenti proteici, metaboliti, biomarcatori di carboidrati, biomarcatori genomici (RNA e DNA), biomarcatori cellulari (catturati come pellet cellulare dai fluidi corporei) e biomarcatori di imaging. Questi tipi di biomarcatori possono anche essere indicati rispettivamente come biomarcatori in vitro (derivati dalla diagnostica in vitro) rispetto a biomarcatori in vivo. Un biomarcatore può essere utilizzato per valutare o rilevare una malattia specifica il prima possibile, il rischio di sviluppare una malattia, l'evoluzione di una malattia e può anche essere predittivo.
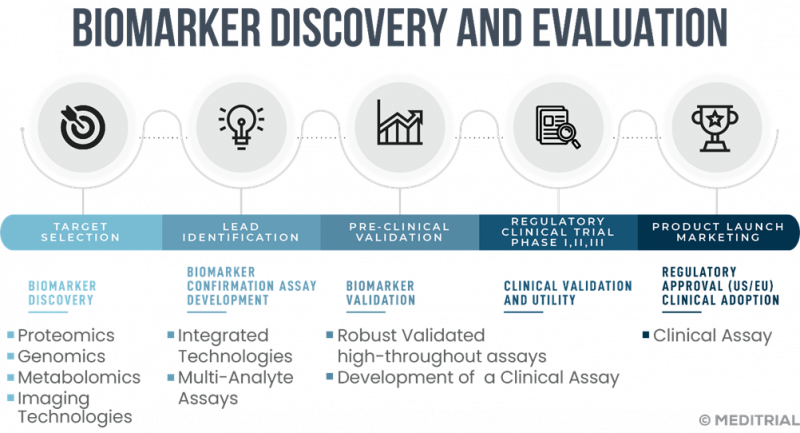
La strada che verrà seguita dalla medicina del futuro, che sta transitando dal paradigma reattivo del passato a quello predittivo del futuro è indirizzata dalle 'omics', come scrive il medico Paola Antonini: "Negli ultimi anni il settore dei biomarker nella ricerca e nella pratica clinica ha presentato notevoli progressi. Questi test possono essere utilizzati nello screening, nella diagnosi, nella caratterizzazione e nel monitoraggio delle malattie; come indicatori prognostici; per lo sviluppo di interventi terapeutici individualizzati; per la previsione e il trattamento delle reazioni avverse ai farmaci; per identificare i tipi cellulari; e per studi farmacodinamici e dose-risposta. L’identificazione di biomarker affidabili può contribuire fortemente allo sviluppo di nuove terapie ed aumentare le percentuali di successo degli studi clinici. Con il passaggio ad un modello di studio più personalizzato, è possibile progettare protocolli dedicati unicamente ai pazienti con maggiori probabilità di rispondere al trattamento. Nella pratica clinica, questo approccio consente di fornire cure personalizzate, più sicure ed efficaci". Il processo di scoperta e validazione di nuovi biomarcatori antiaging è stato studiato dai chimico clinici Alexander Hartmann et al. (vedi bibliografia) i quali, analizzando la letteratura scientifica alla ricerca di biomarcatori, hanno concluso che, a causa della complessità del fenomeno d'invecchiamento, sarà probabilmente difficile condensare in un solo 'biomarcatore standardizzato (composito) dell'invecchiamento' la valutazione predittiva del fenomeno. Per il momento occorre prendere atto che più marcatori possono completarsi a vicenda migliorando così il potere predittivo. Scrive Hartmann: "Recenti confronti hanno dimostrato che i biomarcatori compositi (chiamati anche firme di biomarcatori) sono potenzialmente utili come biomarcatori dell'invecchiamento. Belski et al. (2018), Hastings et al. (2019) hanno entrambi dimostrato che le misure composite sono superiori nella previsione degli esiti legati all'età. Belski et al. (2018) hanno testato l'associazione di 7 diversi metodi (3 orologi epigenetici, 3 biomarcatori compositi e lunghezza dei telomeri) con misure di esito come il funzionamento fisico, il declino cognitivo e i segni soggettivi dell'invecchiamento, incluso l'aspetto del viso invecchiato".
Perchè quando l'organismo è giovane non si ammala (tranne pochissimi casi)? Non si ammala, sembra, perchè il sistema immunitario di un giovane riesce a contrastare moltissimi stress ambientali (cattiva alimentazione, alcol, fumo, droghe, traumi psicofisici, virus, ecc.). E perchè un organismo vecchio si ammala? Perchè il processo d'invecchiamento ha fatto perdere alle sue cellule alcune proprietà e sostanze che aveva da giovane e che occorre ripristinare.
Invecchiamento come principale fattore di rischio
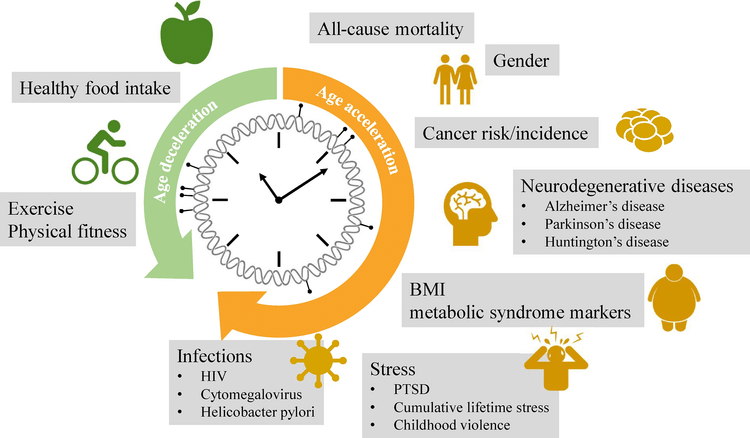
Il biotecnologo Ken Declerck scrive: "L'invecchiamento è il fattore di rischio più importante per le principali malattie dello stile di vita umano, tra cui il cancro, i disturbi neurologici e cardiometabolici. A causa della complessa interazione tra genetica, stile di vita e fattori ambientali, alcuni individui sembrano invecchiare più velocemente di altri, mentre i centenari sembrano avere un processo di invecchiamento più lento. Pertanto, un biomarcatore biochimico che rifletta l'età biologica relativa sarebbe utile per prevedere lo stato di salute di un individuo e il rischio di malattia da invecchiamento. Sebbene sia già noto da anni che i cambiamenti epigenetici cumulativi si verificano con l'invecchiamento, i modelli di metilazione del DNA sono stati usati solo di recente per costruire un predittore dell'orologio epigenetico per l'età biologica, che è una misura di quanto bene funziona il tuo corpo rispetto alla tua età cronologica. Inoltre, la firma epigenetica dell'orologio di metilazione del DNA viene sempre più applicata come biomarcatore per stimare la suscettibilità alle malattie da invecchiamento e il rischio di mortalità. Infine, la firma dell'orologio epigenetico potrebbe essere utilizzata come strumento di gestione dello stile di vita per monitorare l'invecchiamento in buona salute, per valutare gli interventi preventivi contro i disturbi dell'invecchiamento cronico e per prolungare la durata della vita in buona salute.
La dissezione del meccanismo dell'orologio dell'invecchiamento epigenetico fornirà preziose informazioni sul processo di invecchiamento e su come può essere manipolato per migliorare la durata della salute. Recentemente sono state descritte nove caratteristiche cellulari e molecolari dell'invecchiamento (Lopez-Otin et al., 2013). Questi segni distintivi sono: instabilità genomica, logoramento dei telomeri, alterazioni epigenetiche, perdita di proteostasi, rilevamento deregolato dei nutrienti, disfunzione mitocondriale, senescenza cellulare, esaurimento delle cellule staminali e comunicazione intercellulare alterata. È chiaro che questi segni distintivi sono altamente interconnessi e che ulteriori ricerche devono chiarire le relazioni causali tra i segni distintivi e i contributi relativi di ciascun segno distintivo all'invecchiamento. Mentre ogni organismo vivente invecchia e alla fine muore, il tasso di invecchiamento può essere variabile. L'invecchiamento è strettamente correlato al verificarsi di malattie umane. La ricercatrice statistica Paola Sebastiani scrive (2015): "Nel 1980, Fries ipotizzò che mentre gli esseri umani si avvicinano al limite della durata della vita, comprimono il tempo in cui sperimentano le morbilità legate all'età in un periodo sempre più breve prima della morte. Fries ha ipotizzato che questa compressione si verifichi all'età di circa 100 anni. Tuttavia, anche a 100 anni, i centenari sono eterogenei nelle età di insorgenza delle malattie legate all'età e nelle esposizioni ambientali. Non è stato fino a quando non abbiamo analizzato i dati di morbilità longitudinale di persone che vivono oltre 110 anni, che si avvicinano molto meglio alla durata della vita umana, che abbiamo generato risultati a sostegno dell'ipotesi di compressione della morbilità di Fries. Abbiamo dimostrato che in media le persone che sopravvivono fino a 110+ anni trascorrono solo gli ultimi 5 anni della loro vita estremamente lunga con malattie legate all'età che sono associate ad un aumentato rischio di mortalità. Tali individui comprimono anche notevolmente il periodo della loro vita trascorso con la disabilità. Coerentemente con l'ipotesi di compressione della morbilità, le persone che sopravvivono oltre i 105 anni sono anche fenotipicamente molto più simili tra loro rispetto agli individui più giovani che muoiono negli anni '80 e '90". Gli individui con la stessa età cronologica possono avere diversi profili di rischio per le malattie legate all'età. In altre parole, l'età cronologica di due individui può essere la stessa, tuttavia potrebbero esserci differenze significative nella loro età biologica. [...] L'ereditabilità della longevità si aggira intorno al 25%, suggerendo un ruolo importante per i fattori ambientali e di stile di vita (Brooks-Wilson, 2013; Murabito et al., 2012). La variabilità del tasso di invecchiamento è quindi una conseguenza di fattori genetici, di stile di vita, ambientali e di interazione. Un noto e studiato "orologio biologico" è la progressiva perdita di lunghezza dei telomeri durante l'invecchiamento (Sanders e Newman, 2013; Rizvi et al., 2014). I telomeri sono sequenze ripetute alle estremità del cromosoma. Ad ogni divisione cellulare e replicazione del DNA, il telomero si accorcia, il che alla fine porta all'arresto del ciclo cellulare e alla senescenza replicativa. La lunghezza dei telomeri nel sangue è risultata essere un indicatore dell'età cronologica e, curiosamente, era anche associata a malattie, fattori di rischio e mortalità (Sanders e Newman, 2013; Rizvi et al., 2014; Rode et al., 2015). Negli ultimi anni, la metilazione del DNA è stata proposta come predittore più accurato dell'età cronologica (Horvath, 2013; Hannum et al., 2013). La metilazione del DNA è un segno regolatore epigenetico che influenza il fenotipo senza un cambiamento nel genotipo. La metilazione del DNA si riferisce al processo biochimico di aggiunta di un gruppo metilico a un nucleotide di citosina che porta alla formazione di una 5-metilcitosina (5mC). Un aspetto importante della metilazione del DNA è che i cambiamenti sono cumulativi con l'età in risposta a vari stimoli ambientali (Milagro et al., 2013; Lillycrop et al., 2014; Jones et al., 2015). Inoltre, i cambiamenti epigenetici aberranti (epimutazioni) sono stocastici e associati a molteplici malattie e fattori di rischio di malattia al raggiungimento di soglie specifiche (Portela ed Esteller, 2010). In quanto tale, il metiloma del DNA di un individuo è un track record perfetto delle passate esposizioni ambientali e viene letto per monitorare lo stato di salute per stimare il futuro rischio di malattia o l'aspettativa di vita. Il biotecnologo Ken Declerck scrive: "La metilazione del DNA ha superato altri biomarcatori molecolari nella previsione dell'età. Sebbene siano necessarie ulteriori ricerche, studi recenti indicano che l'età della metilazione del DNA potrebbe essere migliore nella stima dell'età biologica piuttosto che dell'età cronologica e potrebbe quindi essere un indicatore promettente per lo stato di salute e malattia."
La metilazione del DNA (meccanismo che, tramite il trasporto di metili, consente alle cellule di regolare l'espressione genetica e perciò di controllare i processi che sono alla base della vita) ha superato altri biomarcatori molecolari nella previsione dell'età. Studi recenti indicano che l'età della metilazione del DNA è un indicatore promettente per lo stato di salute e malattia.
Orologio epigenetico
La firma dell'orologio epigenetico potrebbe essere utilizzata come strumento di gestione dello stile di vita per monitorare l'invecchiamento in buona salute, per valutare gli interventi preventivi contro i disturbi dell'invecchiamento cronico e per prolungare la durata della vita in buona salute. La dissezione del meccanismo dell'orologio dell'invecchiamento epigenetico fornirà preziose informazioni sul processo di invecchiamento e su come può essere manipolato per migliorare la durata della salute.
Come avviene la metilazione del DNA
L'ematologa Anna Reale scrive:"Il DNAm è un marchio epigenetico, presente praticamente in tutti i regni eucariotici, ed è funzionalmente associato al modello di espressione genica e allo sviluppo dell'organismo ( Aliaga et al., 2019 , Skinner, 2011 ). In questo processo biologico , i gruppi metilici vengono trasferiti alla posizione C-5 delle citosine del DNA , culminando nella sintesi di 5-metilcitosina (5mC) nei dinucleotidi CpG palindromi (siti CG) ( Greenberg e Bourc'his, 2019 ). Nonostante formino una piccola frazione dell'intero genoma dei mammiferi (<2%), le regioni ricche di siti CG di circa 1 kb, le cosiddette isole CpG , sono strettamente incorporate in oltre i due terzi dei promotori genici dei mammiferi annotati. Attraverso i 28 milioni di siti CG del genoma umano, circa il 60-80% è costantemente metilato nelle cellule somatiche , mentre il pezzo residuo delle posizioni del genoma CG comprende citosine non metilate ( Edwards et al., 2010 , Illingworth et al., 2010 ). Nonostante 5mC sia rilevato prevalentemente in siti ricchi di CG, ci sono alcune eccezioni come i neuroni umani e le cellule staminali embrionali , che mostrano una metilazione intragenica non CG ( Jang et al., 2017 ). Questa reazione è catalizzata dall'attività degli enzimi DNA metiltransferasi DNMT1 , 3A e 3B (DNMT), che legano in modo covalente la porzione metilica alle citosine ( Jones, 2012 ). Da un punto di vista evolutivo, il meccanismo della metilazione della citosina non si trova in molti eucarioti.
Il DNAm dei mammiferi è determinato e configurato in tre fasi distinte: costituzione (de novo DNAm), mantenimento e rimozione di 5mC ( Li e Zhang, 2014 ).
In primo luogo, la costituzione di DNAm è determinata dall'attività di due metiltransferasi, DNMT3A e DNMT3B, che danno forma allo specifico modello di metilazione genomica per ciascuna cellula germinale o cellula somatica. Questo passaggio è fondamentale, poiché coordina il corretto DNAm dell'intero genoma dopo la demetilazione globale nelle cellule germinali primordiali e negli embrioni precoci, un processo necessario per il ritorno della pluripotenza dopo la specificazione e la fecondazione delle cellule germinali.
Dalla Farmaceutica alla Nutraceutica
La nutrizionista clinica Darija Vranesić-Bender scrive: "Un ampio gruppo di sostanze tra cui vitamine, carotenoidi, flavonoidi e minerali hanno caratteristiche antiossidanti clinicamente significative in vitro o in vivo. C'è un grande interesse per le sostanze antietà derivate dal cibo, e gli ingredienti più popolari sono gli antiossidanti, in particolare il coenzima Q10, i fitoestrogeni, probiotici e acidi grassi omega-3. Queste sostanze hanno effetti benefici sul sistema digestivo e immunitario e modulano i processi infiammatori e degenerativi dell'organismo. La sfida del futuro sarà la combinazione strategica di cosmeceutici e nutraceutici per intervenire nei processi di invecchiamento biologico e nei cambiamenti degenerativi della pelle".
I nutraceutici intesi come categoria specifica di integratori. In questo caso, le sostanze farmacologicamente attive sono estratte dall’alimento che le contiene e all’occorrenza modificate, potenziate o private di eventuali molecole dannose. Si trovano sul mercato sotto forma di capsule, compresse, tinture o polveri
DNA Solutions scrive: "Il termine nutraceutico (coniato dal Dott. Stephen Defelice nel 1989), è l'unione delle parole “nutrizione” e “ farmaceutico” . La nutraceutica studia la funzione benefica che molti alimenti hanno sulla salute umana. Gli alimenti nutraceutici sono anche indicati come alimenti funzionali, alimenti farmaceutici o alimenti agricoli. Un nutraceutico è quindi un “alimento-farmaceutico”, cioè un alimento salutare che unisce ai suoi componenti nutrizionali le proprietà curative di principi attivi naturali estratti da piante di provata e riconosciuta efficacia. Occorre distinguere tra alimenti veri e propri (alimenti funzionali) e i loro singoli componenti ridotti a concentrati o pastiglie detti "nutraceutici". Ma perché assumere nutraceutici? Non sarebbe possibile introdurre queste sostanze consumando alimenti funzionali? Sicuramente sì, ma è molto difficile determinare l'esatta " dose curativa " contenuta negli alimenti di questi principi attivi. Il vantaggio dei preparati nutraceutici risiede proprio nella controllabilità delle quantità assunte. Quando si parla di Nutraceutici non si parla dei soliti integratori vitaminici che si trovano in commercio ma di prodotti che sono alimenti con proprietà terapeutiche. Le sostanze biologiche che le compongono, solitamente concentrate, hanno caratteristiche preventive, riequilibranti, terapeutiche e protettive".

Punto chiave di questa pagina
INVECCHIAMENTO SANO E LONGEVITÀ: La genetista Angela Brooks-Wilson (vedi bibliografia 2013) scrive: "La longevità e l'invecchiamento sano sono tra i fenotipi più complessi studiati fino ad oggi. L'ereditabilità dell'età alla morte in età adulta è di circa il 25%". Ciò suggerisce un'alta influenza dei fattori ambientali nel determinare la longevità. Sempre Angela Brooks-Wilson scrive: " L'epigenetica sta rapidamente emergendo come un aspetto critico dell'invecchiamento e della longevità. I centenari ritardano i cambiamenti di metilazione legati all'età e possono trasmettere questa capacità di conservazione della metilazione alla loro prole. I fattori non genetici, in particolare lo stile di vita, influenzano chiaramente lo sviluppo delle malattie legate all'età e influenzano la salute e la durata della vita nella popolazione generale.
Punti di riflessione
Un biomarcatore è una caratteristica definita e misurabile dei normali processi biologici o patologici o della risposta ad intervento terapeutico. (FDA)
-
Siamo sulla via di un cambiamento radicale nel modo in cui cerchiamo, diagnostichiamo e trattiamo le malattie. Il nostro approccio imperfetto alla medina, basato innanzitutto sui sintomi, sta per cambiare. Interverremo prima che compaiano i sintomi. Molto prima. Interverremo anche prima di "sentirci male". Molte malattie, in fin dei conti, sono geneticamente rilevabili molto prima che diventino sintomatiche. In un futuro molto prossimo, l'analisi personale proattiva del DNA sarà una pratica di routine come lavarci i denti. (David Sinclair p. 186)
-
Fatte da ingranaggi, interruttori, pompe e rotori grandi pochi milionesimi di millimetro, possono muoversi, trasportare farmaci oppure essere comandate a distanza, e grazie alle loro proprietà potranno imprimere una svolta radicale in medicina e nello sviluppo di nuovi materiali, utili anche per produrre le batterie del futuro. Parola del premio Nobel per la Chimica 2016 James Fraser Stoddart, ospite al Politecnico di Milano per una lectio magistralis. (ANSA)
_
La proteomica e la metabolomica, le discipline più “a valle” tra tutte le scienze “omiche”, sono da considerarsi quelle più vicine all’espressione fenotipica di un organismo, poiché rispecchiano sia l’informazione contenuta nel codice genetico sia le influenze derivate dall’interazione con l’ambiente. [...] L’approccio delle scienze omiche apre la strada ad una medicina più personalizzata grazie alla possibilità di predire il decorso della malattia, di determinare la terapia specifica e la risposta al trattamento sulla base del profilo individuale.(Angela Cervesato)
-
La scoperta delle molecole che ho descritto in queste pagine può essere attribuita a un grande colpo di fortuna. Ma pensate cosa il mondo scoprirebbe ora che stiamo attivamente e intenzionalmente ricercando molecole che impegnano le nostre difese innate. Eserciti di chimici stanno adesso lavorando per creare e analizzare molecole naturali e sintetiche che hanno la potenzialità di essere persino migliori nel sopprimere il rumore epigenomico e nel riprogrammare il nostro paesaggio epigenetico. Ci sono centinaia di composti che hanno dimostrato il loro potenziale in questo campo e centinaia di migliaia di altri che aspettano di essere studiati. (David Sinclair p. 145)
-
La conoscenza dettagliata, convergente nella "omica" integrata (genomica, trascrittomica, proteomica e metabolomica), detiene un immenso potenziale per comprendere il meccanismo delle malattie, facilitarne la diagnosi precoce, selezionare strategie terapeutiche personalizzate e valutarne l'efficacia. (Emiro Nemutlu)
-
A quanto pare, nessuna nuova legge è necessaria per spiegare la vita. Su scala nanometrica, la vita è semplicemente una serie ordinata di reazioni chimiche, che concentrano e assemblano atomi che normalmente non sarebbero mai assemblati, o che disgregano molecole che normalmente non si disintegrebbero mai. La vita fa questo utilizzando Pac-Men proteici chiamati enzimi, composti da avvolgimenti a spirale e intrecci stratificati di catene di amminoacidi. Gli enzimi rendono possibile la vita approfittando di movimenti molecolari fortuiti. Ogni secondo che noi viviamo, migliaia di molecole di glucosio vengono catturate entro ciascuna dei nostri trilioni di cellule da un enzima chiamato glucochinasi, che unisce le molecole di glucosio ad atomi di fosforo, i quali le identificano per la produzione di energia. (David Sinclair p. 117)
-
Come dimostra magnificamente la clonazione, le nostre cellule trattengono la loro informazione digitale giovanile anche quando sono vecchie. Per diventare di nuovo giovani, dobbiamo solo trovare uno smalto per rimuovere i graffi. Io lo ritengo possibile. (David Sinclair p. 23)
-
Una delle principali differenze tra gli studi sulla longevità e sull'invecchiamento sano è che la prima si concentra sulla durata della vita, mentre il secondo si concentra sulla durata della salute. La durata della vita e la durata della salute sono intimamente correlate, tuttavia, e gli individui che vivono eccezionalmente a lungo tendono anche a essere sani per gran parte della loro vita. Uno studio fondamentale sulla salute di ultracentenari (età compresa tra 110 e 119 anni), semisupercentenari (età compresa tra 105 e 109 anni), centenari (in questo contesto età compresa tra 100 e 104 anni), novantenni e controlli più giovani ha rilevato che maggiore è la fascia di età, maggiore è la ritardo nell'insorgenza della malattia principale (Andersen et al. 2012). Sorprendentemente, per ogni categoria di età crescente, l'hazard ratio per ciascuno dei sei disturbi (cancro, malattie cardiovascolari (CVD), demenza, ipertensione, osteoporosi e ictus) era <1,0 rispetto al successivo gruppo più anziano. Questo ritardo nello sviluppo della malattia e il rinvio del declino cognitivo e fisico nel gruppo più anziano equivaleva a una compressione della morbilità (Fries 1980). Sulla base di questi risultati, Andersen et al. (2012) suggeriscono che un limite realistico e pratico della durata della vita umana è di 110-115 anni, vicino a quello della persona più anziana documentata al mondo fino ad oggi, che visse fino a 122 (Robine e Allard 1998). (Angela Brooks-Wilson)
_
L'epigenetica sta rapidamente emergendo come un aspetto critico dell'invecchiamento e della longevità. I centenari ritardano i cambiamenti di metilazione legati all'età e possono trasmettere questa capacità di conservazione della metilazione alla loro prole, probabilmente tramite varianti genetiche che influenzano i QTL di metilazione. (Angela Brooks-Wilson)
-
Un aspetto fondamentale della vita umana è la costruzione di relazioni affettive, sessuali e di coppia. Le persone che rimangono sole, per divorzio o per morte del coniuge, presentano, alcune settimane dopo questa perdita, una riduzione dell'attività del sistema immunitario. (Francesco Bottaccioli Epigenetica e Psiconeuroendocrinoimmunologia p.105)
-
-
Il genetista del Sinclair Lab, Yuancheng Lu, ha creato una miscela di tre dei quattro " fattori Yamanaka ", cellule cutanee adulte umane che sono state riprogrammate per comportarsi come cellule staminali embrionali o pluripotenti, in grado di svilupparsi in qualsiasi cellula del corpo. Il cocktail è stato iniettato nelle cellule gangliari della retina danneggiate nella parte posteriore degli occhi di topi ciechi e attivato alimentando i topi con antibiotici. Esercizio, mangiare bene, dormire bene: i 3 migliori modi per prevenire così tante malattie. “L'antibiotico è solo uno strumento. Potrebbe essere davvero qualsiasi sostanza chimica, solo un modo per essere sicuri che i tre geni siano accesi". (Sandee LaMotte)
-
La nostra vita inizia quando un ovulo fecondato si divide e forma nuove cellule che, a loro volta, si dividono anch'esse. Queste cellule sono identiche all'inizio, ma diventano sempre più varie nel tempo. Per molto tempo si è pensato che una cellula matura o specializzata non potesse tornare a uno stato immaturo, ma ora questo si è dimostrato errato. Nel 2006, Shinya Yamanaka è riuscito a identificare un piccolo numero di geni all'interno del genoma dei topi che si sono rivelati decisivi in questo processo. Una volta attivate, le cellule della pelle dei topi potrebbero essere riprogrammate in cellule staminali immature, che a loro volta possono crescere in diversi tipi di cellule all'interno del corpo. (Shinya Yamanaka)
-
Credo che in futuro ritardare e invertire l'invecchiamento sarà il modo migliore per curare le malattie che affliggono la maggior parte di noi. (David Sinclair)
-
Le risposte cellulari alle rotture del DNA a doppio filamento erodono il panorama epigenetico. Questa perdita di informazioni epigenetiche accelera i segni distintivi dell'invecchiamento. Questi cambiamenti sono reversibili mediante riprogrammazione epigenetica. Manipolando l'epigenoma, l'invecchiamento può essere spinto avanti e indietro. (David Sinclair et al. 2023)
-
Un clamoroso studio rafforza la teoria secondo cui l’invecchiamento sarebbe un processo in primo luogo epigenetico e dunque reversibile. L’approccio sperimentale usato dà risultati stimolanti, ma la realtà biologica è probabilmente più complicata e l’elisir di giovinezza non è dietro l’angolo. (Anna Meldolesi)
Il biotecnologo Ken Declerck scrive: "L'invecchiamento è il fattore di rischio più importante per le principali malattie dello stile di vita umano, tra cui il cancro, i disturbi neurologici e cardiometabolici. A causa della complessa interazione tra genetica, stile di vita e fattori ambientali, alcuni individui sembrano invecchiare più velocemente di altri, mentre i centenari sembrano avere un processo di invecchiamento più lento.
Una piattaforma per trasformare l'assistenza sanitaria

Frontiers Health è rapidamente diventata una delle principali conferenze nello spazio della salute digitale, combinando un mix unico di partecipanti e relatori provenienti da fondi di investimento, società di scienze della vita, hub di innovazione sanitaria, compagnie assicurative e start-up di salute digitale, fornendo un'unica piattaforma di esperienze per discutere di come le innovazioni nei rispettivi campi stanno convergendo per reinventare e trasformare l'assistenza sanitaria.
Il futuro sta andando verso la medicina predittiva
Il futuro della medicina si sta indirizzando verso la previsione delle malattie prima che compaiano i primi sintomi, in modo che si possa intervenire con largo anticipo. Si tratterà di una medicina predittiva anzichè reattiva, come avvenuto finora, e questa possibilità si baserà sull'analisi del genoma e sull'uso di molti nuovi biomarcatori. Cos'è un biomarcatore? La definizione che ne dà l'ente statunitense FDA (Food and Drug Administration), che regola la protezione della salute pubblica analogamente a quanto in Europa avviene con l'EMA (Agenzia Europea per i Medicinali), è la seguente: "Un biomarcatore è una caratteristica definita e misurabile dei normali processi biologici o patologici o della risposta ad intervento terapeutico".
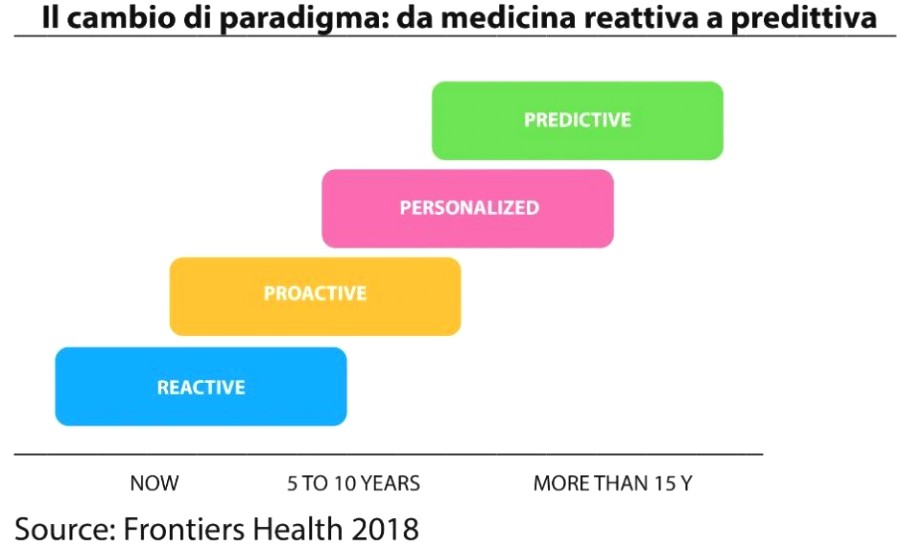
Il giornalista scientifico Dino Biselli, descrivendo l'esito della conferenza 'Frontiers Health 2018', scrive:
Non deve sorprendere che una delle innovazioni maggiormente sotto i riflettori durante Frontiers Health sia stata quella delle digital therapeutics, vale a dire quelle app che, al pari di un farmaco o medical device tradizionali, non solo hanno come fine la prevenzione, la gestione o il trattamento di una patologia, ma vengono anche sottoposte ad un rigoroso percorso scientifico che ne dimostri il suo benefico impatto sul paziente prima della loro immissione in commercio. [...] Le digital therapeutics potranno essere sviluppate per essere dedicate sia ad aspetti legati all’ambito preventivo sia a quelli diagnostici e di trattamento, presidiando tutti i vari passaggi che caratterizzano il patient journey. Ciò significa che il paziente assumerà un ruolo sempre più attivo nella gestione della propria salute e per tale motivo dovrà essere “educato” a monitorare i propri parametri vitali e ad agire in autonomia per gestire al meglio gli smartdevice che avrà a sua disposizione.
Molte tipologie di biomarkers
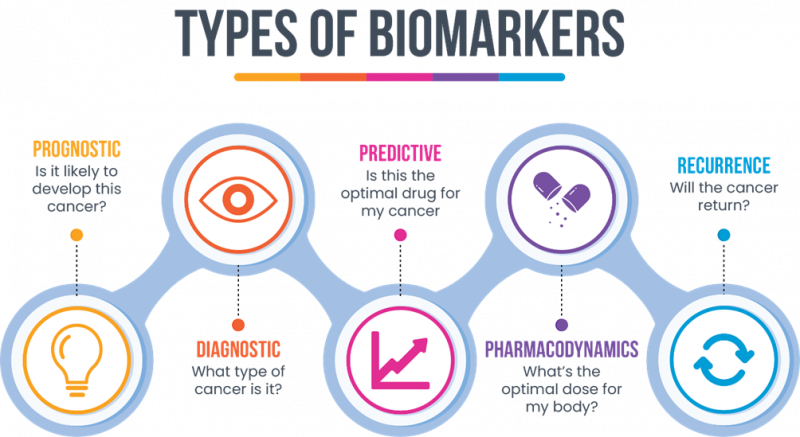
I biomarker possono essere costituiti da DNA, RNA, proteine, metaboliti misurati da campioni di sangue, urina o saliva, liquidi biologici e da tessuti come anche le masse tumorali. Tipologie: Prognostici (individuano la probabilità che 'quel' paziente ha di sviluppare una malattia); Diagnostici (individuano il tipo di malattia sviluppata); Predittivi (individuano la terapia più efficace); Farmacodinamici (individuano il corretto dosaggio della terapia); Recurrence (individuano la probabilità di ricomparsa della malattia)
Il medico Paola Antonini (vedi bibliografia 2022), scrive:
Negli ultimi anni il settore dei biomarker nella ricerca e nella pratica clinica ha presentato notevoli progressi. Questi test possono essere utilizzati nello screening, nella diagnosi, nella caratterizzazione e nel monitoraggio delle malattie; come indicatori prognostici; per lo sviluppo di interventi terapeutici individualizzati; per la previsione e il trattamento delle reazioni avverse ai farmaci; per identificare i tipi cellulari; e per studi farmacodinamici e dose-risposta. L’identificazione di biomarker affidabili può contribuire fortemente allo sviluppo di nuove terapie ed aumentare le percentuali di successo degli studi clinici. Con il passaggio ad un modello di studio più personalizzato, è possibile progettare protocolli dedicati unicamente ai pazienti con maggiori probabilità di rispondere al trattamento. Nella pratica clinica, questo approccio consente di fornire cure personalizzate, più sicure ed efficaci. L’FDA definisce il biomarker come una caratteristica definita e misurabile dei normali processi biologici o patologici o della risposta ad intervento terapeutico. È possibile distinguere biomarker di sicurezza e di efficacia:
I biomarker possono essere costituiti da DNA, RNA, proteine, metaboliti misurati da campioni di sangue, urina o saliva, liquidi biologici e da tessuti come anche le masse tumorali. Mentre i biomarker quantitativi forniscono valori distribuiti su una scala continua, alcuni biomarker di natura qualitativa forniscono un risultato binario (presente o assente). La distinzione tra individui positivi ai biomarker e negativi ai biomarker è effettuata sulla base di un valore di soglia (o cut-off) applicato alle misurazioni quantitative, che spesso è determinato attraverso studi su campioni analizzati retrospettivamente.Di seguito viene fornita una classificazione dei biomarker:
- Biomarker prognostici: un biomarker è definito prognostico quando è in grado di fornire informazioni sulla storia della malattia, indipendentemente dalle terapie che il paziente riceve. I biomarker prognostici sono in grado di indicare il probabile esito di una malattia, in assenza di un intervento terapeutico. Può essere usato come strategia di arricchimento (Enriched Clinical Trials) per selezionare i pazienti che potrebbero avere risultati clinici interessanti o progredire rapidamente.
- Biomarker predittivo: un biomarker è predittivo quando fornisce informazioni sull’attività di specifiche terapie consentendo, quindi, di stratificare i pazienti in base alla loro probabilità o meno di rispondere a un determinato trattamento. Anche questi marcatori possono essere impiegati come strategia di arricchimento degli studi clinici, per identificare una sottopopolazione che potrebbe avere una risposta favorevole o sfavorevole ad un trattamento.
- Biomarker farmacodinamici: questi biomarker aiutano a determinare gli effetti farmacologici di un farmaco e possono fornire indicazione sull’efficacia del trattamento. La maggior parte dei biomarker farmacodinamici, è principalmente impiegato durante gli studi di fase II per comprendere meglio come impiegare un farmaco e guidare nella scelta della dose (Proof-of-concept e dose-ranging studies). Difficilmente vengono impiegati come base per l’approvazione regolatoria.
I dati della ricerca clinica trasposti nella pratica clinica indicano come l’accuratezza nella validazione di un biomarker sia fondamentale per il beneficio del paziente. Un risultato falso positivo esporrà i pazienti a trattamenti non necessari e inefficaci, mentre un risultato falso negativo potrebbe comportate la sospensione di un trattamento potenzialmente efficace. Nuove metodologie basate sulla genetica, metabolomica e proteomica permettono di avere a disposizione un consistente numero di nuovi biomarker. Il loro utilizzo nella ricerca clinica è una realtà in atto, mentre l’uso nella pratica clinica è ancora parziale. Per l’applicazione nella routine clinica, è necessario disporre di raccomandazioni scientifiche per ciascun biomarker, basate su robuste evidenze di correlazione e coerenza con gli eventi clinici nella patologia in esame.
La Rivoluzione omica (omics): genomica, trascrittomica, proteomica, metabolomica
La nefrologa Angela Cervesato (vedi bibliografia 2022) scrive:
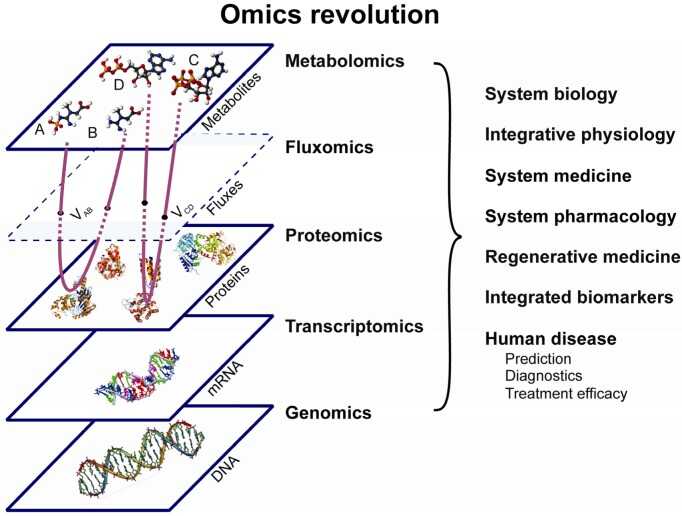
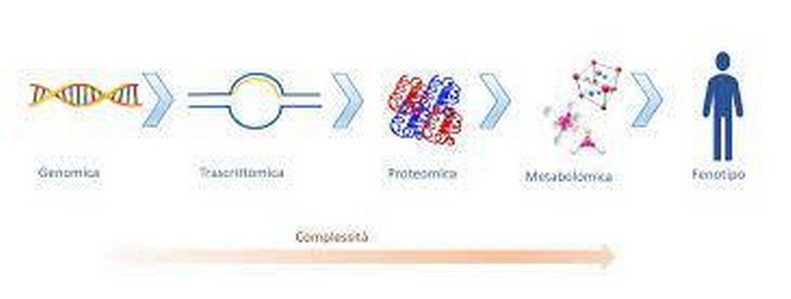
Le scienze “omiche” sono discipline che permettono di indagare le diverse classi di componenti biologiche (geni, trascritti, proteine e metaboliti) di un organismo, di un tessuto, di un campione biologico, nella loro globalità (Figura 1). Esse comprendono: la genomica, lo studio dell’intero set di geni; la trascrittomica, lo studio dei livelli di mRNA; la proteomica, lo studio della traduzione proteica, inteso come l’intero set di proteine (proteoma); la metabolomica, lo studio del metaboloma, definito come l’insieme di metaboliti (piccole molecole con peso molecolare <1,5 kDa. I diversi livelli funzionali analizzati dalle scienze “omiche” sono integrati tra loro nel contesto della systems biology, un innovativo approccio allo studio dei sistemi biologici che si affianca all’approccio ‘’riduzionistico” della biologia tradizionale. La consapevolezza che un sistema biologico sia maggiore della somma delle sue parti e che il suo funzionamento non possa essere rispecchiato dalla funzione di un singolo componente ha promosso l’avvento di strategie di studio di tipo “olistico”. Questo nuovo approccio non sostituisce ma integra la biologia tradizionale, fornendo una visione globale di un sistema biologico o di un organismo.
Tecnologia Point-of-care (POC) in alternativa alla centralizzazione
Vivianne Landry et al. (vedi bibliografia 2022), scrivono:
La tecnologia Point-of-care (POC) offre una comoda alternativa all'analisi di laboratorio centralizzata di campioni biologici. La tecnologia POC consente di eseguire e analizzare rapidamente determinati test molecolari e antigenici ovunque in un ambiente vicino al paziente, come nelle case dei pazienti o al loro capezzale. I biofluidi o biomarcatori liquidi sono particolarmente adatti ai test POC. Non solo i biofluidi sono una ricca fonte di proteine molecolari e peptidi, ma la loro raccolta è anche relativamente semplice e minimamente invasiva. Ad esempio, i biomarcatori salivari sono stati proposti per rilevare e monitorare le malattie infiammatorie e infettive, inclusi i disturbi infiammatori cronici (ad esempio, infiammazione intestinale e condizioni parodontali) e le infezioni sessualmente trasmesse (ad esempio, HIV e HPV). L'accuratezza diagnostica dei biomarcatori molecolari, tuttavia, deve essere rigorosamente stabilita prima che passino alla convenienza dei test POC. Un numero crescente di biomarcatori liquidi è stato associato a malattie delle vie aeree. Il tratto delle vie aeree comprende gli organi coinvolti nella respirazione, nella parola e nella deglutizione, inclusi naso, cavità orale, faringe, laringe, trachea, bronchi e polmoni. Le malattie delle vie aeree e polmonari possono includere condizioni ostruttive delle vie aeree come asma o broncopneumopatia cronica ostruttiva (BPCO), malattie infettive come COVID-19 e irritazione chimica cronica come il reflusso delle vie aeree, noto anche come reflusso laringofaringeo (LPR). Le vie aeree umane sono rivestite di liquido superficiale delle vie aeree, che svolge un ruolo importante nell'eliminazione delle tossine ambientali e nella difesa contro le particelle estranee. I biofluidi locali (ad es. saliva, espettorato, muco, ecc.) si prestano quindi naturalmente come una comoda fonte di biomarcatori liquidi delle vie aeree.
Il check up antiaging proposto da A.M.I.A.
L'Associazione dei medici italiani antiaging (A.M.I.A.) dà un'ampia descrizione dei test e dei trattamenti possibili a chi vuole conoscere il proprio grado di invecchiamento e i trattamenti possibili. Le conclusioni a cui giunge sono: "La scienza ha oramai dimostrato quello che l’esperienza e la tradizione ci avevano fatto intuire: l’età anagrafica ha solo un valore burocratico; l’età più veritiera e specchio fedele del processo di invecchiamento è rappresentata dall’età biologica. Il check-up antiaging ci consente di scoprire “l’età delle nostre cellule”, conseguenza di come stanno invecchiando primariamente i tre sistemi cardine dell’organismo: il sistema nervoso, il sistema endocrino e quello immunitario, tutti intimamente correlati tra loro. (Prof. Dr. Damiano Galimberti)"
Cos'è l'epigenoma
NIH scrive: L'epigenoma è una moltitudine di composti chimici che possono dire al genoma cosa fare. Il genoma umano è l'insieme completo del DNA (acido desossiribonucleico) - circa 3 miliardi di paia di basi - che rende ogni individuo unico. Il DNA contiene le istruzioni per costruire le proteine che svolgono una varietà di funzioni in una cellula. L'epigenoma è costituito da composti chimici e proteine che possono attaccarsi al DNA e dirigere azioni come attivare o disattivare i geni, controllando la produzione di proteine in particolari cellule. Quando i composti epigenomici si attaccano al DNA e ne modificano la funzione, si dice che hanno "marcato" il genoma. Questi segni non cambiano la sequenza del DNA. Piuttosto, cambiano il modo in cui le cellule usano le istruzioni del DNA. I segni vengono talvolta trasmessi da una cellula all'altra mentre le cellule si dividono. Possono anche essere tramandati da una generazione all'altra.
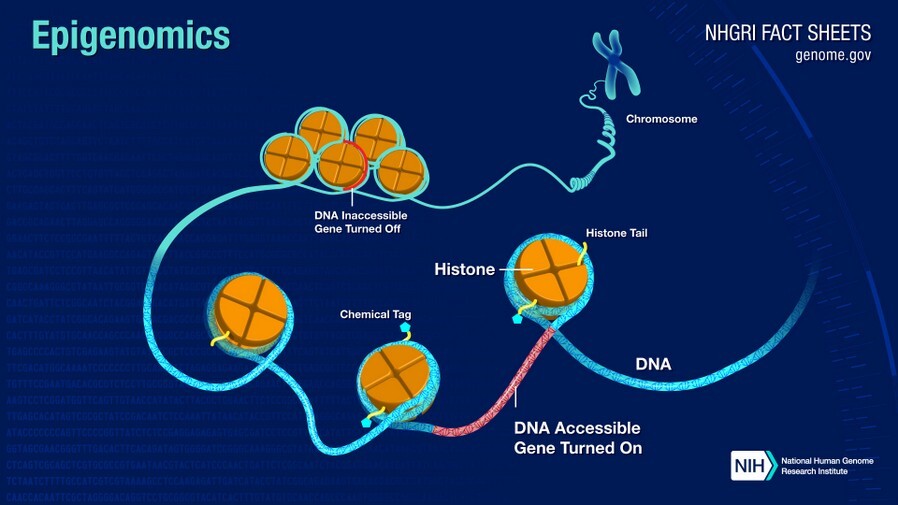
L'epigenoma governa l'invecchiamento delle nostre cellule e viene danneggiato dal cattivo stile di vita
Tutti gli esseri viventi sperimentano un aumento dell'entropia, che si manifesta come una perdita di informazioni genetiche ed epigenetiche.
Il genetista David Sinclair ed altri (vedi bibliografia 2023) scrive:
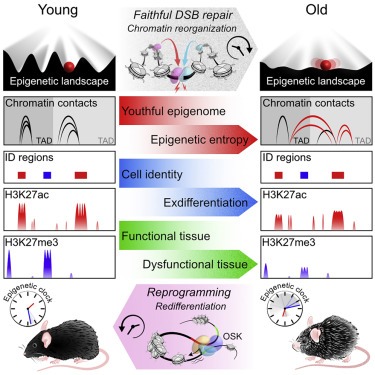
Usando un sistema chiamato "ICE" (modifiche inducibili all'epigenoma), scopriamo che l'atto di fedele riparazione del DNA fa avanzare l'invecchiamento a livello fisiologico, cognitivo e molecolare, inclusa l'erosione del paesaggio epigenetico, l'esdifferenziazione cellulare, la senescenza e l'avanzamento di l'orologio di metilazione del DNA, che può essere invertito dal ringiovanimento mediato da OSK.
L'articolo, pubblicato su Cell, è stato riassunto e commentato dal giornalista Sandee LaMotte su CNNhealth (vedi bibliografia 2023), che scrive:
Gli esperimenti combinati, pubblicati per la prima volta giovedì sulla rivista Cell , sfidano la convinzione scientifica che l'invecchiamento sia il risultato di mutazioni genetiche che minano il nostro DNA, creando una discarica di tessuto cellulare danneggiato che può portare al deterioramento, alla malattia e alla morte.
"Non è spazzatura, non è un danno che ci fa invecchiare", ha detto Sinclair, che ha descritto il lavoro l'anno scorso a Life Itself, un evento di salute e benessere presentato in collaborazione con la CNN.“Crediamo che sia una perdita di informazioni — una perdita della capacità della cellula di leggere il suo DNA originale così da dimenticare come funzionare — più o meno allo stesso modo in cui un vecchio computer può sviluppare software corrotto. Io la chiamo la teoria dell'informazione dell'invecchiamento. Jae-Hyun Yang, ricercatore di genetica presso il Sinclair Lab e coautore dell'articolo, ha affermato di aspettarsi che i risultati "trasformeranno il modo in cui vediamo il processo di invecchiamento e il modo in cui ci avviciniamo al trattamento delle malattie associate all'invecchiamento". Mentre il DNA può essere visto come l'hardware del corpo, l'epigenoma è il software. Gli epigeni sono proteine e sostanze chimiche che si trovano come lentiggini su ciascun gene, in attesa di dire al gene "cosa fare, dove farlo e quando farlo." L'epigenoma accende e spegne letteralmente i geni. Tale processo può essere innescato da inquinamento, tossine ambientali e comportamenti umani come fumare, seguire una dieta infiammatoria o soffrire di una cronica mancanza di sonno.E proprio come un computer, il processo cellulare si corrompe man mano che più DNA viene rotto o danneggiato, ha detto Sinclair. "La cellula va nel panico e le proteine che normalmente controllano i geni vengono distratte dal dover andare a riparare il DNA", ha spiegato. "Poi non tornano tutti al punto di partenza, In altre parole, i pezzi cellulari perdono la strada di casa. "La scoperta sorprendente è che c'è una copia di backup del software nel corpo che è possibile ripristinare", ha detto Sinclair. "Stiamo mostrando perché quel software viene danneggiato e come possiamo riavviare il sistema attingendo a un interruttore di ripristino che ripristina la capacità della cellula di leggere di nuovo correttamente il genoma, come se fosse giovane".Non importa se il corpo ha 50 o 75 anni, sano o distrutto dalla malattia, ha detto Sinclair. Una volta innescato quel processo, “il corpo poi ricorderà come rigenerarsi e sarà di nuovo giovane, anche se sei già vecchio e hai una malattia. Una delle nostre scoperte è stata quella di renderci conto che se si utilizza questo particolare set di tre cellule staminali pluripotenti, i topi non tornano all'età zero, il che causerebbe il cancro o peggio", ha detto Sinclair. “Invece, le cellule tornano tra il 50% e il 75% dell'età originaria, si fermano e non ringiovaniscono, il che è una fortuna. Come le cellule sappiano farlo, non lo capiamo ancora.Oggi, il team di Sinclair sta cercando di trovare un modo per fornire l'interruttore genetico in modo uniforme a ciascuna cellula, ringiovanendo così l'intero topo in una volta."La consegna è un ostacolo tecnico, ma altri gruppi sembrano aver fatto bene", ha detto Sinclair, indicando due studi non pubblicati che sembrano aver superato il problema.
Mentre il DNA può essere visto come l'hardware del corpo, l'epigenoma è il software. L'epigenoma governa l'invecchiamento delle nostre cellule e viene danneggiato dal cattivo stile di vita, ma può essere riparato. In attesa che siano stati validati da FDA gli esiti delle ricerche conviene migliorare il proprio stile di vita per ridurre i fattori infiammatori. Ciò significa: mangiare bene (ad es. dieta mediterranea), bere poco alcol, non fumare, non drogarsi, ridurre i fattori di stress (per quanto possibile).
Conclusioni (provvisorie): Medicina del futuro e Antiaging:
La rivoluzione 'omica' sta portando alla scoperta e utilizzo di nuovi biomarcatori che misureranno l'età biologica umana
La medicina del futuro sta cambiando paradigma, abbandonando il paradigma reattivo per abbracciare quello predittivo. Questo processo è previsto entro 15 anni e avverrà in parallelo con i processi antiaging, sull'onda della rivoluzione 'omica' e dello sviluppo di orologi epigenetici sempre più precisi. Per capire cosa succederà dobbiamo capire com'è fatto l'organismo umano, e quindi il fenotipo. In genetica, il fenotipo (dal greco antico φαίνω (phaínō) 'apparire, mostrare, risplendere', e τύπος (túpos) 'marchio, tipo') è l'insieme delle caratteristiche o tratti osservabili di un organismo. Il termine riguarda la morfologia dell'organismo (forma fisica e struttura), i suoi processi di sviluppo, le sue proprietà biochimiche e fisiologiche. Il fenotipo deriva da due fattori fondamentali: l'espressione del codice genetico dell'organismo (il suo genotipo) e l'influenza dei fattori ambientali. Entrambi i fattori possono interagire, influenzando ulteriormente il fenotipo. Il fenotipo di un organismo non comporterà solo le caratteristiche osservabili come la morfologia, ma includerà anche molecole e strutture come l'RNA e le proteine prodotte come codificate dai geni; questo è indicato come "fenotipo molecolare". La genetista Angela Brooks-Wilson scrive (2013): "L'ereditabilità dell'età alla morte in età adulta è di circa il 25%. L'epigenetica sta rapidamente emergendo come un aspetto critico dell'invecchiamento e della longevità."
Cos'è un fenotipo
"Pheno" significa semplicemente "osservare" e deriva dalla stessa radice della parola "fenomeno". E quindi è una tipologia osservabile di un organismo, e può riferirsi a qualsiasi cosa, da un tratto comune, come l'altezza o il colore dei capelli, alla presenza o all'assenza di una malattia. Ma è importante ricordare che i fenotipi sono ugualmente, o talvolta anche più fortemente influenzati dagli effetti ambientali rispetto agli effetti genetici. Di solito non c'è una correlazione uno a uno tra un genotipo e un fenotipo, perchè ci sono quasi sempre influenze ambientali, quali, ad esempio, ciò che si mangia, quanto ci si esercita fisicamente, quanto si fuma, quanto alcol si beve, ecc. Tutte queste sono influenze ambientali che determineranno il fenotipo.
Che cosa influenza il fenotipo
Per capire di cosa si compone la resilienza di ogni individuo, alla quale è affidato il suo invecchiamento sano, in biologia è in corso la rivoluzione 'omica'. Infatti “Genoma” è una parola ormai piuttosto conosciuta, anche per merito del Progetto Genoma Umano, che 20 anni fa ci ha consegnato la prima bozza della sequenza di lettere che compongono il nostro DNA. Ma se dicessimo “trascrittoma”? Oppure “proteoma” o, ancora, “metaboloma”? Sono parole certo meno familiari, eppure è facile accorgersi che hanno tutte qualcosa in comune e cioè quelle tre lettere finali - oma - che indicano una totalità. Ciascuno di questi termini, dunque, si riferisce all’insieme totale di qualcosa che si può trovare in un tessuto, un organismo o anche una singola cellula. Sono sequenze di DNA per il genoma, trascritti (cioè molecole di Rna) per il trascrittoma, proteine per il proteoma, metaboliti (piccole molecole coinvolte nelle varie vie biochimiche di una cellula) per il metaboloma. E così via. Le tecniche utilizzate per studiare questi insiemi, invece, prendono il nome di "omiche" (genomica, trascrittomica, proteomica ecc.) e rappresentano una delle avanguardie più promettenti della ricerca biologica. La proteomica e la metabolomica, le discipline più “a valle” tra tutte le scienze “omiche”, sono da considerarsi quelle più vicine all’espressione fenotipica di un organismo, poiché rispecchiano sia l’informazione contenuta nel codice genetico sia le influenze derivate dall’interazione con l’ambiente. La metabolomica è stata ideata nel 1970 da Arthur B. Robinson il quale, analizzando i modelli cromatografici "confusi" di urina di soggetti a cui era stata somministrata la Vitamina B6, si rese conto che centinaia o migliaia di costituenti chimici nell'urina contenevano informazioni molto utili. Dal 1971 Robinson ha fatto pubblicare altri diciannove elaborati sui modelli quantitativi degli umori corporei. Queste nuove metodologie basate sulla genetica, metabolomica e proteomica permettono di avere a disposizione un consistente numero di nuovi biomarker. Il loro utilizzo nella ricerca clinica è una realtà in atto, mentre l’uso nella pratica clinica è ancora parziale.
La rivoluzione 'omica'
I progressi nella tecnologia ad alto rendimento offrono nuove opportunità per la ricerca omica per comprendere il processo patologico di varie malattie umane complesse. Le tecnologie single-omics forniscono solo informazioni limitate sui meccanismi biologici delle malattie. DNA, RNA, proteine, metaboliti e microrganismi di solito svolgono ruoli complementari e svolgono insieme determinate funzioni biologiche. Ma cos'è un biomarcatore? Maria Salud Garcia-Gutierrez scrive (vedi bibliografia 2020): "Al fine di armonizzare il termine di biomarcatore, la Food and Drug Administration (FDA) in collaborazione con il NIH Joint Leadership Council ha convocato il gruppo di lavoro sui biomarcatori FDA-NIH nel 2016. Questo gruppo ha semplificato la definizione di biomarcatore essendo considerato come "una caratteristica definita che è misurato come un indicatore di normali processi biologici, processi patogeni o risposte a un'esposizione o intervento”. Questa definizione, più chiara e concisa, definisce un biomarcatore specificandone le principali applicazioni senza inutili complessità o informazioni contraddittorie. Inoltre, per garantirne l'uso clinico, un buon biomarcatore dovrebbe essere misurato con elevata riproducibilità, presentare un rapporto segnale/rumore considerevole e, soprattutto, soddisfare la condizione di essere modificato in modo dinamico e affidabile con il progredire della condizione clinica. Inoltre, un biomarcatore dovrebbe essere accessibile per la sua rilevazione e misurazione, come nel caso di un parametro plasmatico o di un marcatore genetico, o essere rilevato mediante tecniche istologiche o di immagini/neuroimmagini ".
Tipologie di biomarcatori
La strada che verrà seguita dalla medicina del futuro, che sta transitando dal paradigma reattivo del passato a quello predittivo del futuro è indirizzata dalle 'omics', come scrive il medico Paola Antonini: "Negli ultimi anni il settore dei biomarker nella ricerca e nella pratica clinica ha presentato notevoli progressi. Questi test possono essere utilizzati nello screening, nella diagnosi, nella caratterizzazione e nel monitoraggio delle malattie; come indicatori prognostici; per lo sviluppo di interventi terapeutici individualizzati; per la previsione e il trattamento delle reazioni avverse ai farmaci; per identificare i tipi cellulari; e per studi farmacodinamici e dose-risposta. L’identificazione di biomarker affidabili può contribuire fortemente allo sviluppo di nuove terapie ed aumentare le percentuali di successo degli studi clinici. Con il passaggio ad un modello di studio più personalizzato, è possibile progettare protocolli dedicati unicamente ai pazienti con maggiori probabilità di rispondere al trattamento. Nella pratica clinica, questo approccio consente di fornire cure personalizzate, più sicure ed efficaci". Il processo di scoperta e validazione di nuovi biomarcatori antiaging è stato studiato dai chimico clinici Alexander Hartmann et al. (vedi bibliografia) i quali, analizzando la letteratura scientifica alla ricerca di biomarcatori, hanno concluso che, a causa della complessità del fenomeno d'invecchiamento, sarà probabilmente difficile condensare in un solo 'biomarcatore standardizzato (composito) dell'invecchiamento' la valutazione predittiva del fenomeno. Per il momento occorre prendere atto che più marcatori possono completarsi a vicenda migliorando così il potere predittivo. Scrive Hartmann: "Recenti confronti hanno dimostrato che i biomarcatori compositi (chiamati anche firme di biomarcatori) sono potenzialmente utili come biomarcatori dell'invecchiamento. Belski et al. (2018), Hastings et al. (2019) hanno entrambi dimostrato che le misure composite sono superiori nella previsione degli esiti legati all'età. Belski et al. (2018) hanno testato l'associazione di 7 diversi metodi (3 orologi epigenetici, 3 biomarcatori compositi e lunghezza dei telomeri) con misure di esito come il funzionamento fisico, il declino cognitivo e i segni soggettivi dell'invecchiamento, incluso l'aspetto del viso invecchiato".
Invecchiamento come principale fattore di rischio
Il biotecnologo Ken Declerck scrive: "L'invecchiamento è il fattore di rischio più importante per le principali malattie dello stile di vita umano, tra cui il cancro, i disturbi neurologici e cardiometabolici. A causa della complessa interazione tra genetica, stile di vita e fattori ambientali, alcuni individui sembrano invecchiare più velocemente di altri, mentre i centenari sembrano avere un processo di invecchiamento più lento. Pertanto, un biomarcatore biochimico che rifletta l'età biologica relativa sarebbe utile per prevedere lo stato di salute di un individuo e il rischio di malattia da invecchiamento. Sebbene sia già noto da anni che i cambiamenti epigenetici cumulativi si verificano con l'invecchiamento, i modelli di metilazione del DNA sono stati usati solo di recente per costruire un predittore dell'orologio epigenetico per l'età biologica, che è una misura di quanto bene funziona il tuo corpo rispetto alla tua età cronologica. Inoltre, la firma epigenetica dell'orologio di metilazione del DNA viene sempre più applicata come biomarcatore per stimare la suscettibilità alle malattie da invecchiamento e il rischio di mortalità. Infine, la firma dell'orologio epigenetico potrebbe essere utilizzata come strumento di gestione dello stile di vita per monitorare l'invecchiamento in buona salute, per valutare gli interventi preventivi contro i disturbi dell'invecchiamento cronico e per prolungare la durata della vita in buona salute.
La dissezione del meccanismo dell'orologio dell'invecchiamento epigenetico fornirà preziose informazioni sul processo di invecchiamento e su come può essere manipolato per migliorare la durata della salute. Recentemente sono state descritte nove caratteristiche cellulari e molecolari dell'invecchiamento (Lopez-Otin et al., 2013). Questi segni distintivi sono: instabilità genomica, logoramento dei telomeri, alterazioni epigenetiche, perdita di proteostasi, rilevamento deregolato dei nutrienti, disfunzione mitocondriale, senescenza cellulare, esaurimento delle cellule staminali e comunicazione intercellulare alterata. È chiaro che questi segni distintivi sono altamente interconnessi e che ulteriori ricerche devono chiarire le relazioni causali tra i segni distintivi e i contributi relativi di ciascun segno distintivo all'invecchiamento. Mentre ogni organismo vivente invecchia e alla fine muore, il tasso di invecchiamento può essere variabile. L'invecchiamento è strettamente correlato al verificarsi di malattie umane. La ricercatrice statistica Paola Sebastiani scrive (2015): "Nel 1980, Fries ipotizzò che mentre gli esseri umani si avvicinano al limite della durata della vita, comprimono il tempo in cui sperimentano le morbilità legate all'età in un periodo sempre più breve prima della morte. Fries ha ipotizzato che questa compressione si verifichi all'età di circa 100 anni. Tuttavia, anche a 100 anni, i centenari sono eterogenei nelle età di insorgenza delle malattie legate all'età e nelle esposizioni ambientali. Non è stato fino a quando non abbiamo analizzato i dati di morbilità longitudinale di persone che vivono oltre 110 anni, che si avvicinano molto meglio alla durata della vita umana, che abbiamo generato risultati a sostegno dell'ipotesi di compressione della morbilità di Fries. Abbiamo dimostrato che in media le persone che sopravvivono fino a 110+ anni trascorrono solo gli ultimi 5 anni della loro vita estremamente lunga con malattie legate all'età che sono associate ad un aumentato rischio di mortalità. Tali individui comprimono anche notevolmente il periodo della loro vita trascorso con la disabilità. Coerentemente con l'ipotesi di compressione della morbilità, le persone che sopravvivono oltre i 105 anni sono anche fenotipicamente molto più simili tra loro rispetto agli individui più giovani che muoiono negli anni '80 e '90". Gli individui con la stessa età cronologica possono avere diversi profili di rischio per le malattie legate all'età. In altre parole, l'età cronologica di due individui può essere la stessa, tuttavia potrebbero esserci differenze significative nella loro età biologica. [...] L'ereditabilità della longevità si aggira intorno al 25%, suggerendo un ruolo importante per i fattori ambientali e di stile di vita (Brooks-Wilson, 2013; Murabito et al., 2012). La variabilità del tasso di invecchiamento è quindi una conseguenza di fattori genetici, di stile di vita, ambientali e di interazione. Un noto e studiato "orologio biologico" è la progressiva perdita di lunghezza dei telomeri durante l'invecchiamento (Sanders e Newman, 2013; Rizvi et al., 2014). I telomeri sono sequenze ripetute alle estremità del cromosoma. Ad ogni divisione cellulare e replicazione del DNA, il telomero si accorcia, il che alla fine porta all'arresto del ciclo cellulare e alla senescenza replicativa. La lunghezza dei telomeri nel sangue è risultata essere un indicatore dell'età cronologica e, curiosamente, era anche associata a malattie, fattori di rischio e mortalità (Sanders e Newman, 2013; Rizvi et al., 2014; Rode et al., 2015). Negli ultimi anni, la metilazione del DNA è stata proposta come predittore più accurato dell'età cronologica (Horvath, 2013; Hannum et al., 2013). La metilazione del DNA è un segno regolatore epigenetico che influenza il fenotipo senza un cambiamento nel genotipo. La metilazione del DNA si riferisce al processo biochimico di aggiunta di un gruppo metilico a un nucleotide di citosina che porta alla formazione di una 5-metilcitosina (5mC). Un aspetto importante della metilazione del DNA è che i cambiamenti sono cumulativi con l'età in risposta a vari stimoli ambientali (Milagro et al., 2013; Lillycrop et al., 2014; Jones et al., 2015). Inoltre, i cambiamenti epigenetici aberranti (epimutazioni) sono stocastici e associati a molteplici malattie e fattori di rischio di malattia al raggiungimento di soglie specifiche (Portela ed Esteller, 2010). In quanto tale, il metiloma del DNA di un individuo è un track record perfetto delle passate esposizioni ambientali e viene letto per monitorare lo stato di salute per stimare il futuro rischio di malattia o l'aspettativa di vita. Il biotecnologo Ken Declerck scrive: "La metilazione del DNA ha superato altri biomarcatori molecolari nella previsione dell'età. Sebbene siano necessarie ulteriori ricerche, studi recenti indicano che l'età della metilazione del DNA potrebbe essere migliore nella stima dell'età biologica piuttosto che dell'età cronologica e potrebbe quindi essere un indicatore promettente per lo stato di salute e malattia."
Dalla Farmaceutica alla Nutraceutica
La nutrizionista clinica Darija Vranesić-Bender scrive: "Un ampio gruppo di sostanze tra cui vitamine, carotenoidi, flavonoidi e minerali hanno caratteristiche antiossidanti clinicamente significative in vitro o in vivo. C'è un grande interesse per le sostanze antietà derivate dal cibo, e gli ingredienti più popolari sono gli antiossidanti, in particolare il coenzima Q10, i fitoestrogeni, probiotici e acidi grassi omega-3. Queste sostanze hanno effetti benefici sul sistema digestivo e immunitario e modulano i processi infiammatori e degenerativi dell'organismo. La sfida del futuro sarà la combinazione strategica di cosmeceutici e nutraceutici per intervenire nei processi di invecchiamento biologico e nei cambiamenti degenerativi della pelle". DNA Solutions scrive: "Il termine nutraceutico (coniato dal Dott. Stephen Defelice nel 1989), è l'unione delle parole “nutrizione” e “ farmaceutico” . La nutraceutica studia la funzione benefica che molti alimenti hanno sulla salute umana. Gli alimenti nutraceutici sono anche indicati come alimenti funzionali, alimenti farmaceutici o alimenti agricoli. Un nutraceutico è quindi un “alimento-farmaceutico”, cioè un alimento salutare che unisce ai suoi componenti nutrizionali le proprietà curative di principi attivi naturali estratti da piante di provata e riconosciuta efficacia. Occorre distinguere tra alimenti veri e propri (alimenti funzionali) e i loro singoli componenti ridotti a concentrati o pastiglie detti "nutraceutici". Ma perché assumere nutraceutici? Non sarebbe possibile introdurre queste sostanze consumando alimenti funzionali? Sicuramente sì, ma è molto difficile determinare l'esatta " dose curativa " contenuta negli alimenti di questi principi attivi. Il vantaggio dei preparati nutraceutici risiede proprio nella controllabilità delle quantità assunte. Quando si parla di Nutraceutici non si parla dei soliti integratori vitaminici che si trovano in commercio ma di prodotti che sono alimenti con proprietà terapeutiche. Le sostanze biologiche che le compongono, solitamente concentrate, hanno caratteristiche preventive, riequilibranti, terapeutiche e protettive".
per scaricare le conclusioni (in pdf):
Bibliografia (chi fa delle buone letture è meno manipolabile)
- Elisa Buson (2019), Le macchine molecolari rivoluzionarie come gli aerei
- Paola Antonini (2022), Studi clinici, così i biomarker aiutano la ricerca - Aboutpharma
- Vivianne Landry, Patrick Coburn, Karen Kost, Xiyu Liu, Nicole YK Li-Jessen (2022), Diagnostic Accuracy of Liquid Biomarkers in Airway Diseases: Toward Point-of-Care Applications
- Angela Cervesato et al. (2020), La proteomica e la metabolomica nello studio delle malattie genetiche del rene: dai big data alla medicina di precisione (PDF) [3 citazioni]
- (2021), La rivoluzione omica - Telethon
- Phenotype - Biology online
- I Biomarkers dell’Aging - A.M.I.A.
- Alexander Hartmann et al. (2021), Ranking Biomarkers of Aging by Citation Profiling and Effort Scoring - Frontiers
- Ken Declerck, Wim Vanden Berghe (2018), Back to the future: Epigenetic clock plasticity towards healthy aging (PDF) [66 citazioni]
- Anna Reale et al. (2022), Counteracting aged DNA methylation states to combat ageing and age-related diseases
- (2017), What are Biomarkers? CD Creative Diagnostic
- Grannum R. Sant et al. (2017), Live-single-cell phenotypic cancer biomarkers-future role in precision oncology? - npj
- Emirhan Nemutlu, Song Zhang, Nenad Juranic (2012), 18O-assisted dynamic metabolomics for individualized diagnostics and treatment of human diseases - Research Gate
- Angela Brooks-Wilson (2013), Genetics of healthy aging and longevity [230 citazioni]
- Joanne Murabito, Rong Yuan, Kathryn Lunetta (2012), The search for longevity and healthy aging genes: insights from epidemiological studies and samples of long-lived individuals [201 citazioni]
- Darija Vranesić-Bender (2010), The role of nutraceuticals in anti-aging medicine - PubMed
- Bhanushree Gupta et al. (2019), Nutraceuticals for antiaging
- Gil Atzmon et al. (2004), Clinical Phenotype of Families with Longevity
- S.S. Kunizeva et al. (2022), Current Trends and Approaches to the Search for Genetic Determinants of Aging and Longevity
- Elena Dusi (2010), Tutti i geni dei centenari arriva il test della longevità - La Repubblica
- Nutraceutica: definizione, significato ed esempi - Coohesion
- Sandee La Motte (2023), Old mice grow young again in study. Can people do the same? CNN
- David Sinclair et Al. (2023), Loss of epigenetic information as a cause of mammalian aging - Cell
- Anna Meldolesi (2023), Topi geneticamente ringiovaniti: la vecchiaia ha davvero gli anni contati? - Le Scienze
- (2022), Fattori Yamanaka e riprogrammazione cellulare parziale - AlmaPhysio
Guarda le pagine correlate
Scrivi, se non sei d'accordo
Se ritenete che le tesi del "punto chiave" non vengano sufficientemente supportate dagli argomenti presenti in questa pagina potete esprimere il vostro parere (motivandolo).
Inviate una email con il FORM. Riceverete una risposta. Grazie della collaborazione.
Libri consigliati
a chi è interessato a capire la genetica e l'epigenetica
a chi è interessato a capire la genetica e l'epigenetica
Spesa annua pro capite in Italia per gioco d'azzardo 1.583 euro, per l'acquisto di libri 58,8 euro (fonte: l'Espresso 5/2/17)
Pagina aggiornata il 16 marzo 2023